FDA, 18 SENE SONRA BİR ALZHEİMER İLACINA ONAY VERDİ
Dikkat: Yazının sonunda ek var!
***
FDA, 18 sene sonra ilk defa bir Alzheimer ilacına onay verdi.
Karar, bağımsız danışma komitesinin muhalefetine ve ilacın hastalara yardımcı olabileceğine dair yeterli delil olmadığını söyleyen bazı Alzheimer uzmanlarına rağmen alındı.
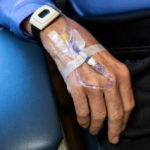
Aduhelm adıyla satılacak olan ve aducanumab etken maddeli ilaç hafif hafıza ve düşünme sorunları olan kişilerde bilişsel gerilemeyi yavaşlatmayı amaçlıyor ve ayda bir damardan veriliyor.
FDA, ilacın klinik denemelerinin etkinliği göstermek için eksik deliller sağladığını kabul ederek, üretici Biogen’in yeni bir klinik araştırma yürütmesi şartıyla onay verdi.
Buna “hızlandırılmış onay” adı veriliyor ve ciddi hastalığı olan hastaların tedaviden mahrum kalmamasını amaçlıyor.
Birkaç sene sürmesi beklenen faz 4 çalışmasından beklenen netice alınamazsa onay geri alınabilecek ama bu arada ilacı alanlar da tedavinin üzerine bir bardak soğuk su içmiş olacaklar.
Biogen’in CEO’su Michel Vounatsos, onayı “tarihi bir an” olarak nitelendiriyor ve ilacın “Alzheimer hastalığıyla yaşayan insanların tedavisini değiştireceğine ve gelecek yıllarda sürekli yenilikleri tetikleyeceğine” inandığını söylüyor.
CEO, bu sözleri söylerken muhtemelen ellerini ovuşturuyor olmalıdır.
Çünkü delillerin ilacın etkili olup olmadığı konusunda önemli şüpheler uyandırdığını söyleyen birçok uzman var.
Bunlar, ilaç bazı hastalarda bilişsel gerilemeyi yavaşlatabilse bile, sağladığı faydanın çok az olacağını ve ilacın beyinde şişme veya kanama gibi yan etkilerinin daha riskli olabileceğini dile getiriyorlar.
Biogen’ in bu ilaçtan milyar dolarlar kazanması bekleniyor zira bir hastanın senelik tedavi maliyetinin 10.000-50.000 dolar arasında olacağı tahmin ediliyor.
USA’ da 6 milyon ve tüm dünyada da 30 milyon Alzheimer hastası olduğuna ve her geçen zaman hasta sayısı katlanarak arttığına göre Biogen’ in şimdiden köşeyi döndüğü söylenebilir.
Bugün için USA’ da Alzheimer’ in çeşitli evreleri için bilişsel azalmayı geciktireceği öne sürülen beş ilaç var.
İlacın prospektüsünde ilacın beyin şişmesi, mikro kanamalar ve baş ağrısı gibi yan etkilerini takip etmek için tedaviden önce ve tedavinin altıncı ve on ikinci aylarında MR yapılması gerektiği yazıyor.
Monoklonal bir antikor olan aducanumab Alzheimer hastalarının beyinlerinde biriken ve amiloid adı verilen bir proteini hedef alıyor ve tedavi ile beyinde amiloid miktarı azalıyor.
Ne var ki bu hastalığın iyileşmesi anlamına gelmiyor. Daha önce amiloid miktarını azaltan pek çok ilacın belirtiler üzerine etkisi olmadığı anlaşıldı.
Kaynak: https://www.nytimes.com/2021/06/07/health/fda-approves-alzheimers-drug.html
***
EK 1 (11.6.2021): USA’ da sağlık profesyonellerinin CDC ve FDA gibi dünya tıbbına yön ve akıl veren kuruluşlarına olan güvenlerinin %77 ve %51 azaldığı tespit edildi. Benim güvenimde en ufak bir azalma yok çünkü bunlara zaten güvenmiyordum.
***
EK 2 (11.6.2021): Harvardlı profesör, FDA’nın tartışmalı alzheimer ilacını onaylamasının ardından istifa etti: ABD tarihindeki en kötü kararlardan biri.
ABD Gıda ve İlaç İdaresi’nin (FDA) Çevresel ve Merkezi Sinir Sistem Danışma Komitesi’nin üçüncü bir üyesi, kurumun Biogen’in yeni alzheimer ilacı Aduhelm’i onaylama konusundaki tartışmalı kararı üzerine istifa etti. Harvard Tıp Okulu’nda nöroloji profesörü olan Dr. Aaron Kesselheim, FDA’nın Biogen hakkındaki kararının ” ABD’nin yakın tarihindeki en kötü ilaç onay kararı olduğunu” söyledi. İstifa mektubu sunanlar arasında Kesselheim’in yanı sıra, Mayo Clinic nöroloğu Dr. David Knopman ve Washington Üniversitesi nöroloğu Dr. Joel Perlmutter da yer alıyor.
Kesselheim,“FDA, son dakikada ilacın beyin amiloidi üzerindeki etkisinin Alzheimer hastalarına yardımcı olacağı şeklindeki tartışmalı önermeye dayanarak, İnceleme sürecini “Hızlandırılmış Onay” a çevirdi. FDA’nın Komitenin bilimsel tavsiyelerini onay kararlarına yeterince entegre etme yeteneğine sahip olmadığının benim için oldukça açık. Söz konusu karar, alzheimer hastalarının bakımını, FDA’ya olan kamu güvenini, faydalı terapötik yenilik arayışını ve sağlık sisteminin baltalayacaktır” ifadelerini kullandı.
Biogen’in hisseleri yüzde 38 arttı
Diğer taraftan, Biogen’in hisseleri, FDA’nın biyoteknoloji şirketinin ilacını onaylamasının ardından Pazartesi günü yüzde 38 arttı.
Aduhelm adlı ilaç, yaklaşık 20 yılın ardından, ABD düzenleyicileri tarafından alzheimer ile yaşayan kişilerde bilişsel gerilemeyi yavaşlatmak için onaylanan ilk ilaç oldu. Biogen’in ilacı, beyinde beta-amiloid olarak bilinen ve bilim insanlarının yıkıcı hastalıkta rol oynamasını beklediği “yapışkan” bir bileşiği hedef alıyor.
Kanser ilaçları için kullanılan “hızlandırılmış onay” verildi
FDA, ilacı Alzheimer hastalarında bilişsel gerilemeyi yavaşlatacağı beklentisiyle, genellikle kanser ilaçları için kullanılan hızlandırılmış onay adı verilen bir program kapsamında onayladı. Kurum, ilaca Biogen’in başka bir klinik araştırma yürütmesi şartıyla onay verdiğini duyurdu. Öte yandan, istifa eden bilim insanları FDA’nın Çevresel ve Merkezi Sinir Sistem Danışma Komitesi’nin kararlarını dikkate almadığını öne sürdü. Komite aynı zamanda, kurum personelini, verileri aşırı derecede olumlu bir şekilde gözden geçirdiği için de eleştirdi.
İstifa eden danışman sayısı 3’e yükseldi
Ajansın ilaca ilişkin kararının bir sonucu olarak şimdiye kadar FDA’nın Çevresel ve Merkezi Sinir Sistem Danışma Komitesi’nden üç kişi istifa etti. İstifa mektubu sunanlar arasında Kesselheim’in yanı sıra, Mayo Clinic nöroloğu Dr. David Knopman ve Washington Üniversitesi nöroloğu Dr. Joel Perlmutter yer alıyor.
“Hayal kırıklığına uğradım”
Knopman,“Danışma komitesinin girdilerinin FDA tarafından nasıl ele alındığı konusunda çok hayal kırıklığına uğradım. Bir daha böyle bir duruma düşmek istemiyorum” dedi. Bununla birlikte, FDA’nın bilimsel olarak aducanumab da olarak bilinen ilacı hızlı bir şekilde kullanmak isteyen Alzheimer hastalarının arkadaşlarından ve aile üyelerinden yoğun bir baskıyla karşı karşıya kaldı. Ancak, ilaç 2016’da umut vaat ettiğinden beri düzenleyici onaya giden yol tartışmalı oldu.
2019’un Mart ayında Biogen, bağımsız bir grup tarafından yapılan bir analiz olumsuz sonuçlandıktan sonra ilaçla ilgili çalışmalarını durdurdu. Ancak, şirket birkaç ay sonra ilaç için düzenleyici onayı isteyeceğini açıklayarak yatırımcıları şok etti. Biogen 2019’un sonlarında ilaç için onay istediğinde, bilim insanları daha büyük bir veri setinin yeni bir analizinin Aduhelm’in “erken Alzheimer hastalığı olan hastalarda klinik bakım ihtiyacını azalttığını” gösterdiğini söyledi.
***
EK 3 (7.7.2021): Alzheimer hastalığı olan insanlar ve aileleri, sahte umuda değil, umuda ihtiyaç duyar. Aducanumab’ın onayı, bu tartışmayı çözmek için çok az şey yaparken, hastalar, klinisyenler ve araştırmacılar için faydasız belirsizliklere yol açıyor. Bazıları aducanumab’ı amiloid kaskad teorisinin bir delili olarak görüyor; milyarlarca liraya mal olan, onlarca yıl süren başarısız araştırmaları ve binlerce katılımcıyı deneysel tedavilerin yan etkilerine maruz bırakılmasını haklı çıkarıyor. Bazıları, bunun sadece anti-amiloid tedavilere boşuna yatırımı teşvik edeceğinden, fonları fiziksel aktiviteyi iyileştirmek veya hipertansiyonu azaltmak ve teşhisten sonra daha iyi destek gibi etkili önleyici tedbirlerden uzaklaştıracağından endişe ediyor.
Kaynak: https://www.bmj.com/content/374/bmj.n1682
***
EK 4 (17.7.2021): USA’ nın iki önemli tıp merkezi Cleveland ve Mont Sınai, Alzheimer ilacı Aduhelm’i kullanmayı reddetti. Bu, ilacın FDA tarafından onaylanması konusundaki endişelerin açık bir işaretidir. Kaynak: https://www.nytimes.com/2021/07/14/health/cleveland-clinic-aduhelm.html
***
EK 5 (20.12.2021): Avrupa İlaç Ajansı (EMA), Alzeheimer hastalığına karşı geliştirilen yeni bir ilacın kullanımını onaylamadı. EMA, Aducanumab ilacının Alzheimer semptomlarının erken tespit edildiği vakalarda etkili olmadığını açıkladı. Alzheimer üzerine çalışma yapan kurumlar bu verilen karardan memnun olmadıklarını, binlerce kişi için önemli bir tedavi seçeneğinin yok edildiğini söyledi. 20 yıl sonra ilk kez Alzheimer hastalığına yeni bir tedavi imkanı sunan Aducanumab ilacı, ABD’de Haziran ayında tartışmalı bir şekilde onaylamıştı.
Kaynak: https://www.bbc.com/turkce/haberler-dunya-59697436
***
EK 6 (21.12.2021): EMA, Aducanumab ilacının Alzheimer semptomlarının erken tespit edildiği vakalarda etkili olmadığını açıkladı. Alzheimer üzerine çalışma yapan kurumlar bu verilen karardan memnun olmadıklarını, binlerce kişi için önemli bir tedavi seçeneğinin yok edildiğini söyledi. 20 yıl sonra ilk kez Alzheimer hastalığına yeni bir tedavi imkanı sunan Aducanumab ilacı, ABD’de Haziran ayında tartışmalı bir şekilde onaylanmıştı. Bu gelişmelerden sonra Biogen Inc, hastanelerden gelen yüksek maliyetinin faydalarına değmediği yönündeki şikayetleri üzerine, beklenenden daha yavaş ABD satışlarıyla karşı karşıya kaldıktan sonra, Alzheimer ilacının fiyatını yaklaşık yarı yarıya indirerek 28.200 dolara düşürdü.
Kaynak: https://www.medimagazin.com.tr/guncel/genel/tr-tartismali-ilacin-fiyati-da-dustu-11-681-98540.html
***
EK 7 (6.10.2022): 100 yıldan fazla zamandır geleneksel görüş, Alzheimer’ın beyinde amiloid plakların birikmesinden kaynaklandığı idi ama bu çalışma amiloid plakların aslında beyindeki azalan çözünür amiloid-beta seviyelerinin bir sonucu olduğunu iddia ediyor.
Bu seviyeler, biyolojik, metabolik veya enfeksiyona bağlı stres durumlarında normal proteinin anormal amiloid plaklarına dönüşmesi sebebiyle azalıyor.
Araştırmacılar daha önce beyinde plak oluşumundan bağımsız olarak, çözünür amiloid-beta düzeyi yüksek olan kişilerin bilişsel olarak normal olduğunu ama protein düzeyi düşük olanların bilişsel bozulmaya sahip olma ihtimalinin daha yüksek olduğunu göstermişlerdi.
Kaynak: https://content.iospress.com/articles/journal-of-alzheimers-disease/jad220808
Makale: High Soluble Amyloid-β42 Predicts Normal Cognition in Amyloid-Positive Individuals with Alzheimer’s Disease-Causing Mutations
***
EK 9 (2.3.2024): Biogen’in 31 Ocak’ta Alzheimer için anti-amiloid ajan aducanumab’ın (Aduhelm) geliştirilmesine ve ticarileştirilmesine son vereceğini açıkladı. Aducanumab, kendi danışma panelinin ilacı onaylamama tavsiyesine rağmen Haziran 2021’de FDA’ dan hızlandırılmış onay almıştı.
Makale: Biogen’s Abandonment of Controversial Alzheimer’s Drug Is No Surprise, Experts Say
***
EK 9 (23.10.2024): İngiltere, yaşlıların dolandırılmasına dur dedi!
İngiltere’ de NICE (bizdeki karşılığı Türkiye İlaç ve Tıbbi Cihaz Kurumu=TİTCK) Alzheimer ilacı donanemab’ ı, sağladığı “nispeten küçük faydanın” maliyetinden fazla olmaması sebebiyle reddetti.
Taslak kılavuzda, klinik araştırma verilerinin, aylık enjeksiyonun hafif Alzheimer hastalığında hastalığın ilerlemesini dört ila yedi ay yavaşlatabileceğini öne sürmekle beraber, aylık damar yoluyla uygulanan ilacın maliyetinin çok yüksek olduğu, yan etkilerinin yoğun bir şekilde izlenmesi gerektiği bildiriliyor.
Rehbere göre, “Klinik çalışmalardan elde edilen deliller, mevcut tedaviye donanemab eklenmesiyle bilişsel işlevin zamanla kötüleşmeye devam ediyor, uzun vadeli etkilerine dair yeterli veri de bulunmuyor.
O kirli beyninizi çekin yaşlılardan. İlacı siz kullanın, belki aklınız başınıza gelir.
K: https://www.bmj.com/content/387/bmj.q2342
Makale: NICE rejects Alzheimer’s drug donanemab owing to cost and “significant health risks”
***















Alzheimer ilacı olamaz.
NEDENİ vardır: Beyin hücrelerinin insülin ve leptin direncidir.
Önlenirse kimse Alzheimer hastası olmaz.
FDA gene şirketlere hizmet etmeye devam ediyor. İşe yaramayan önceki ilaçların patenti bitti ve de ucuzladı mesele budur!
Sayın Uğur Dündar, SÖMÜRGE EKONOMİSİ modeli diyor.
Ben de; SÖMÜRGE EĞİTİMİ, SÖMÜRGE MEDYASI ve de SÖMÜRGE TIBBI diyorum.