BURUN YOLUYLA VERİLEN AŞILAR AĞIR HASTALIK VE BULAŞMAYI ÖNLÜYOR, KALICI BAĞIŞIKLIK SAĞLIYOR

Dikkat: Yazının sonunda ek var!
***
Bugün tüm dünyada yüz milyonlarca doz uygulanan Kovid-19 aşılarının tamamı kas içine zerk suretiyle yapılıyor.
Bu uygulama, antikor ve hücresel bağışıklık sağlayarak ağır hastalık, hastaneye yatış ve ölümleri yüzde 95’ e varan oranlarda önlemekle beraber enfeksiyonu ve dolayısıyla da bulaşmayı önleyemiyor.
Antikorlar virüsün akciğerlerde çoğalmasını ve hasarı azaltır ama burundaki çoğalmaya etkileri azdır. Virüs, sistemik antikor tedavisine rağmen burunda günlerce kalır (1).
Pandeminin tam olarak kontrol altına alınabilmesi ancak enfeksiyonu da önleyebilen aşılarla mümkündür ve bu aşıların temel hususiyeti de üst solunum yollarına uygulanması ve böylece de lokal bağışıklığı uyarmasıdır (2, 3, 4, 5).
Burun yoluyla uygulanan vektör aşısı
Science Advances’ da yayınlanan araştırmada burun yoluyla uygulanan bir vektör aşısının sistemik doğuştan ve edinsel immun cevaplarla beraber lokal bağışıklık (IgA) da sağladığı gösterildi (6).
Fare ve gelinciklerde yapılan deneylerde, parainfluenza virüsüne (PIV5) Kovid-19’ un S proteininin (CVXGA1) eklendiği aşı burun yoluyla uygulandı.
Aşıda sitoplazmik kuyruğu PIV5 F proteini ile değiştirilen S proteinin tamamı bulunuyordu.
Tek doz aşının, ağır enfeksiyonların görüldüğü K18-hACE2 türü farelerde, virüs enfeksiyonunu, virüsün bulaşması ve enfeksiyonları önlediği, hücresel ve antikor bağışıklığı sağladığı belirlendi.
Burun yoluyla uygulama koronavirüslerin üst solunum yollarında üremesini ve hastalığın alt solunum yolları ve akciğerlere sirayetini engelliyor.
PIV5, daha önce grip, kuduz ve RSV aşılarında vektör olarak kullanılmıştır. Hayvan modellerinde emniyetlidir ve herhangi bir hastalıkla ilişkilendirilmemiştir.
Burundan uygulanan aşı kalıcı bağışıklık sağlıyor
Aşılarla ilgili bir başka mesele de antikor nötralizasyonunu azaltan Kovid-19 varyantlarının aşı etkinliğini tehlikeye atabilmesidir.
Bir başka yeni araştırmada da burun yoluyla uygulanan aşıların, orijinal virüs ve ortaya çıkan SARS-CoV-2 varyantlarına karşı “kalıcı koruma” sağladığı gösterildi (7).
Bu çalışmada, aşının farelerde kalıcılığı, doz cevabı ve çapraz koruyucu aktivitesi değerlendirildi.
Tek bir burun içi ChAd-SARS-CoV-2-S dozu, serumda kalıcı olarak yüksek nötralize edici ve Fc efektör antikor cevabı ve kemik iliğinde uzun ömürlü plazma hücrelerini salgılayan S proteinine has IgG ve IgA cevapları sağladı.
100 kat aşı doz aralığında ve 200 günlük bir süre boyunca SARS-CoV-2 suşuna karşı koruma gözlemlendi.
Aşılamadan 6 hafta veya 9 ay sonra, serum antikorları B.1.351, B.1.1.28 ve B.1.617.1 spike proteinleri olan suşları nötralize etti ve varyant virüslere karşı üst ve alt solunum yollarında neredeyse tam koruma sağladı.
Bu sonuçlar, ChAd-SARS-CoV-2-S ile burun yoluyla aşılamanın, orijinal virüs ve ortaya çıkan SARS-CoV-2 suşlarına karşı kalıcı koruma sağladığını gösteriyor.
Hayvanlarda koruyucu etkisi bildirilen, buruna uygulanan S protein bazlı şempanze adenovirüs vektörlü aşısı (ChAd-SARS-CoV-2-S) insanlarda da denenmeye başladı.
Bizde de burun yoluyla uygulanan protein bazlı bir aşı ile yapılan klinik öncesi çalışmalarda aşının varyantlara karşı da etkili olduğu gösterilmiş ve insan çalışmalarına başlanacağı bildirilmişti (8).
Gelelim neticeye
Kas içine zerk edilen aşılar ağır hastalık ve ölümleri önlemekle beraber bulaşmayı azaltsalar bile tam olarak önleyemiyor.
Burun yoluyla uygulanan aşılar ise virüslerin üst solunum yollarında çoğalmaları önledikleri için bulaşmaya da mani oluyorlar.
Lokal bağışıklık sağlayan bu aşıların etkinliklerinin kalıcı olması da çok mühimdir.
Pandemi ancak bu tür aşılarla kontrol altına alınabilir.
Kaynaklar:
1. https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(21)00098-6
6. https://advances.sciencemag.org/content/7/27/eabi5246
7. https://www.cell.com/cell-reports/fulltext/S2211-1247(21)00869-X
Makaleler:
1. Protection of K18-hACE2 mice and ferrets against SARS-CoV-2 challenge by a single-dose mucosal immunization with a parainfluenza virus 5–based COVID-19 vaccine
2. An intranasal vaccine durably protects against SARS-CoV-2 variants in mice

***
EK 1 (26.7.2021): KORCAN AYATA: “En başından beri ağırlık verilmesi gereken “burun aşıları”, faz1’i yeni bitiriyorlar. Solunum yolunda virüsü karşılayıp hastalığı engellemenin ötesinde, virüsün çoğalıp yayılmasını azaltma potansiyeli büyük. Tıpkı doğal bağışıklık gibi.” Kaynak: https://twitter.com/korcanayata/status/1419549429997129728?s=20
***
EK 2 (10.9.2021): Fare deneylerinde, ağız yoluyla uygulanan, sıcağa dayanıklı aşının güçlü mukozal nötralize edici bağışıklık sağladığı gösterildi. Kaynak: https://www.biorxiv.org/content/10.1101/2021.09.09.459634v1
***
EK 3 (12.9.2021): Kas içine zerk edilen aşıların solunum yolu virüslerine karşı lokal T hücresi bağışıklığını indüklemesi beklenmemektedir, ancak daha fazla araştırma yapılması gerektiği açıktır. Kaynak: https://www.frontiersin.org/articles/10.3389/fimmu.2021.745256/full
***
EK 4 (25.9.2021): FERHAT ARSLAN “Ben makalemde aşı yapılmak isteniyorsa 1- Buruna sprey olarak,mukozal ve sistemik toksisiteden uzak 2- Canlı ve zayıflatılmış 3- Sadece risk grubunda (asla çocukları kapsamaz olması gerektiğini yazdım. Var mı böyle bir aşı, yok. Olan inaktive korur mu?“
“Koruyup korumadığını Türkiye verisi ortaya çıkarsa söyleyebiliriz. Veri yoksa ne diyelim. Hepsi boş laf olur. Sabitlenmiş tweet de ki makalemi okuyun.”
“Risk grubu kimdir? KOAH! Kalp yetmezliği, Kötü seyirli Diyabet, Siroz, hemodiyaliz hastaları, nakil hastaları, kanser nedeni ile kemoterapi alanlar, Romatoloji hastalıklar nedeni ile ilaç kullananlar, doğuştan immun yetersizliği olanlar.“
Kaynak: https://twitter.com/Ferhatarslandr/status/1441805645544452101?s=20
“Tekrarlayalım inaktive aşı ile mRna uygulamasını ayrı tutuyorum. Birisi standartları olan ve virüsün çoklu proteinlerine karşı geliştirilen, uzun yıllardır kullanılan teknikle üretilen inaktive aşı.Bunu risk grubu yaptırabilir. Diğeri mRna, güvenlik profili belli değil. Bak bu net.”
“Aşı karşıtı değilim. Baskıya, dayatmaya ve genetik müdahaleye karşıyım. Bu kadar basit.”
Kaynak: https://twitter.com/Ferhatarslandr/status/1441792706070683648?s=20
***
EK 5 (29.9.2021): COVID-19 VACCİNE NASAL SPRAY
University of Oxford researchers are now conducting an open-label clinical trial of the intranasal vaccine in healthy human volunteers.
All COVID-19 vaccines now in use are injected into muscle, producing antibodies that circulate in the blood but aren’t necessarily present in the nose and nasal passages, suggesting that vaccinated individuals could still become infected and transmit the virus. Previous studies in rhesus monkeys showed that the Oxford/AstraZeneca vaccine, which isn’t authorized for use in the US, protected against pneumonia but did not reduce shedding from their upper respiratory tract.
The authors of the new study first compared the injected and the intranasal vaccines in hamsters. Both routes of administration produced high antibody levels, but the nasal spray outperformed the injection.
Vaccinated and unvaccinated hamsters were then exposed to SARS-CoV-2, and both the injected and intranasal vaccines protected hamsters from serious disease.
The researchers then gave 2 doses of the intranasal vaccine to 4 rhesus monkeys, who developed antibody levels similar to those seen in people who’d recovered from COVID-19. The 4 vaccinated monkeys, along with 4 unvaccinated rhesus monkeys, were then exposed to SARS-CoV-2. The vaccinated monkeys had less virus in their noses and lung tissue, and none of them developed symptoms of pneumonia, while 3 of the unvaccinated monkeys did.
Although the observed differences between the animals that received the intranasal vaccine and the ones that didn’t were very encouraging, they weren’t significant, the authors noted. Too few animals were vaccinated to establish clear correlations, they wrote.
Still, senior author Vincent Munster, PhD, of the NIAID’s virology laboratory, said in a statement, “[T]hese results justify additional tests of nasal delivery for COVID-19 vaccines in people.”
Kaynak: https://jamanetwork.com/journals/jama/fullarticle/2784523
***
EK 6 ( 7.10.2021): Spike proteininden hazırlanan ve ağız veya burun yoluyla uygulanan yeni bir vektör aşının hamsterlerde hastalığa karşı koruduğunu ve aşılanmamış, aşısız hamsterlere bulaşmanın azaldığı gösterildi. Aşılanan hayvanlarda güçlü antikor cevabı elde edildi. Daha sonra aşılanmış hamsterler ve plasebo ile aşılanan hamsterler SARS-CoV-2 ile enfekte edildi. Aşılanmış hamsterlerin burun ve akciğerlerinde, viral RNA ve bulaşıcı virüsün azaldığı ve plasebo aşı yapılan hamsterlere göre akciğerlerdeki patolojinin daha hafif olduğu tespit edildi. Aşılanmış ve SARS-CoV-2 ile enfekte hamsterlerle aynı odada kalan aşısız hamsterlerin burun sürüntülerinde daha az viral RNA bulundu ve kontrol grubuna göre hastalık belirtileri de daha az idi. Kaynak: https://www.biorxiv.org/content/10.1101/2021.10.03.462919v1
***
EK 8 (12.5.2022): FERHAT ARSLAN “Şunu söyleyeli yazalı 1.5 yıl oldu. Bak senin anlayacağın dilden yazacağım. Boğazından burnundan girecek bir virüs için kolundan aşı yaptırman hele bir de tekrarlatman bir şeye yaramaz. Adı bilim olan dergiden, buyur bilimci!“
Recall of B cell memory depends on relative locations of prime and boost immunization. Kaynak: https://www.science.org/doi/10.1126/sciimmunol.abn5311
Kaynak: https://twitter.com/Ferhatarslandr/status/1524783354880708608?s=20&t=Gi9FUubqlBPcDA5epNe5tg
***
EK 9 (12.1.2023):Respiratory virus like SARS-COV-2 typically propagate in the mucus: mouth, nose, digestive tract and lungs. For propagation to be stopped in the mucus, notably in the lungs, a preemptive immune arsenal needs to be stimulated there. This is exactly what occurs once recovered from a natural infection:
Kaynak: https://covidmythbuster.substack.com/p/much-ado-about-nothing
Makale: Can a shot in the deltoid stimulate mucus in the airways? The answer is “No” … Then, how can vaccines be effective?
***
EK 10 (5.8.2023): Infectious particles can be shared through aerosols and droplets formed as the result of normal respiration. Whether Abs within the nasal/oral fluids can similarly be shared between hosts has not been investigated. The circumstances of the SARS-CoV-2 pandemic facilitated a unique opportunity to fully examine this provocative idea. The data we show from human nasal swabs provides evidence for the aerosol transfer of Abs between immune and nonimmune hosts.
The simplest interpretation of our results is that 1) aerosol transmission of Ab can occur and that 2) the propensity for this transfer is, unsurprisingly, directly related to the amount of nasal/oral Ab found within those in the population possessing immunity. We have yet to encounter an equally parsimonious interpretation, although admittedly this does not mean one does not exist. The concept of herd immunity is a central tenant of public health vaccination campaigns. Overt blockade of infection as well as a reduction in viral transmission downstream of a breakthrough infection are widely accepted conceptual mechanisms by which vaccination-induced immunity in specific individuals protects nonimmune community members. With this in mind, it stands to reason that aerosol transmission of Abs could also contribute to host protection and represent an entirely unrecognized mechanism by which passive immune protection may be communicated.
As cross-reactivity between seasonal coronavirus spike proteins and the RBD of SARS-CoV-2 has not been observed, we do not believe that our results have been unduly influenced by subjects’ prior exposure to seasonal coronavirus. Although there is some small degree of cross-reactivity between the S2 domains of SARS-CoV-2 and the OC43 seasonal strain (5, 6), this does not extend to the S1 domain or the more limited RBD. Were this to be true, it is arguable that the course of the pandemic would have been substantially altered for the better.
Unfortunately, the difficulty in recruiting participants from unvaccinated households in conjunction with the availability of the vaccines for children under the age of 5 y rendered continued sample acquisition unsustainable. As such, we were unable to determine whether the aerosol transfer of IgA might achieve statistical significance from increased sample evaluation, nor were we able to devise any assay suitable for determining the biological relevance of the observed aerosol transfer of IgG. However, whether Ab transfer mediates host protection will be a function of exposure, and it seems reasonable to suggest, all things being equal, that any amount of Ab transfer would prove useful to the recipient host. With the documented benefits of parental vaccination in reducing the risk of infection in the unvaccinated children in the same home (7), it is tempting to speculate that aerosol-mediated Ab transfer may have possibly contributed to the reported findings. It seems likely that nasal swabs originally collected for monitoring SARS-CoV-2 transmission in this study could be repurposed for examining SARS-CoV-2–specific IgG and IgA within the vaccinated adults as well as noninfected family members, potentially providing the statistical power necessary for validating the conclusions drawn in the current study.
Makale: Evidence for Aerosol Transfer of SARS-CoV-2–Specific Humoral Immunity
***





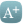










Sağlık Bakanı KOCA:
İnaktif aşıyı daha önemsiyoruz. Çünkü diğer aşıların uzun vadede ilk defa uygulanıyor mRNA aşıları… uzun vadeli sonuçlarını daha bilmiyoruz. O nedenle biz inaktif aşıda ısrar ettik. Bunu açıkça söylüyorum.
https://twitter.com/DindarGenc2/status/1415545563475501057?s=20