KOLESTEROL HAPLARI KASLARI MAHVEDEBİLİYOR

Dikkat: Yazının sonunda ek var!
***
Yeni bir araştırmaya göre, statin kullanımıyla ilişkili olan bir nekrotizan miyopati formu giderek daha fazla görülüyor.
Prag Charles Üniversitesi uzmanları, 2008-2011 seneleri arasında birkaç hastada gördükleri nekrotizan miyopati vakalarının hızla arttığını, 2012-2014 arasında 18 yeni vaka teşhis ettiklerini bildirdi.
Rheumatology’ de on-line olarak yayınlanan araştırma 27 hastada kas biyopsilerinde seyrek lenfositlerle beraber kas lifleri arasında nekroz tespit edildiğini gösteriyor (1).
Bu araştırma, statinlerin ilacın bırakılmasıyla düzelmeyen kas toksisitesinin oto-immun bir formu ile ilişkilendiren delillere bir yenisini eklemiş oluyor.
Farklı bir miyopati
Miyopati olarak bilinen bir grup hastalık, edinsel olarak proksimal kaslarda zayıflık, kreatinin kinaz yüksekliği ve elektromiyografi anormallikleri ile karakterizedir.
Miyopatilerin sebepleri arasında oto-immünite, toksisite, distrofi ve paraneoplastik tutulum vardır.
Birçok vakada klinik ve biyopsi bulguları teşhis için yeterlidir; gerekirse miyozit spesifik oto-antikorlar (signal recognition particle karşı) da bakılabilir.
2010’ da, nekrotizan miyopatisi olan 26 hastanın 16’ sında şimdiye kadar tanımlanmamış olan 200-kd ve 100-kd proteinlerine karşı antikorlar tespit edildi.
Bunların klinik özellikleri ve kas biyopsileri derinlemesine incelendiğinde bu hastaların oto-immün miyopati ailesine dâhil oldukları ve immunsüpresif tedaviye cevap verdikleri belirlendi (2).
Son senelerde polimiyozit benzeri klinik tablo gösteren ama kas biyopsilerinde beklenildiği gibi lenfosit fazlalığının değil nekrozun hâkim olduğu hastalar giderek daha çok görülmeye başlandı.
Anti 200/100 oto-antikorları olan hastalar içinde, klinik belirtileri proksimal kas zayıflığı, yüksek kreatinin kinaz seviyeleri, tipik elektromiyografi bulguları ve immunsüpresif tedaviye müspet cevapla beraber diğer oto-immun miyopatilere benzeyen hastalar vardı.
Bunların iki farklı özelliği vardı: Bazı hastalarda çok yüksek CK seviyelerine karşılık kas zayıflığı çok azdı, yüzde 60’ ı ise kas belirtilerinden önce statin kullanıyordu.
Bir başka araştırmada da oto-immün nekrotizan miyopatisi olan 25 hastanın yüzde 82’ sinin statin kullandıkları ama buna karşılık dermatomiyozitlilerin sadece yüzde 18’ inin polimiyozitlilerin yüzde 24’ ünün statin aldıkları belirlendi (3).
Çoğu statin kullanan bu hastaların prednizon, azathioprin, metotreksat, rituksimab ve IVIG gibi immün süpresif ilaçlarla tedavileri gerekiyor ve çoğuna idame tedavisi uygulanması icap ediyor.
Statin bağlantısı
Statinlerin kolesterol düşürücü etkileri HMGCR (3-hydroxy-3-methylglutaryl-coenzyme A reductase) enzimini bloke etmeleri sebebiyledir.
Statinlerin kas-iskelet belirtilerine yol açtıkları da çok iyi bilinir; bu ilacı kullananların yüzde 20’ sinde kas ağrısı (miyalji) ortaya çıkar.
Statinlerle ilişkilendirilen miyopati doğrudan miyotoksik etkiye bağlıdır ve kendi kendiyle sınırlıdır.
İmmun-mediated nekrotizan miyopati (IMNM) ise oldukça farklı bir tablodur.
Miyopatili hastalarda immun cevap ve statinler arasındaki ilişki statinlerin 200/100 oto-antijenlerin ekspresyonunu artırmasına bağlanıyor.
Statinlerin ~97-kd HMGCR ekspresyonunu artırdığı dikkate alındığında bu enzimin ~100-kd oto-antijen olabileceği de düşünülebilir.
Nitekim anti-200/100-kd pozitif hastaların serumlarının HMGCR’ nin hücre içi katalitik domainini tanıyabildiği gösterilmiştir (4).
Anti-HMGCR antikorlarını tanıyan ELISA yöntemiyle kas belirtileri olan 750 kişilik kohortta bu antikorların %6’ da pozitif olduğu bulundu.
Bu hastalardaki fenotip İMNM ile uyumlu idi ve 50 yaşın üzerinde olanların yüzde 90’ ı statin kullanıyordu.
Çek kohortu
2004-2014 arasında 357 hastaya kas biyopsisi yapıldı ve 233’ üne immun-mediated miyopati (IMM) teşhisi kondu.
Bunların yüzde 38.6’ sında dermatomiyozit ve yüzde 27.9’ unda polimiyozit tespit edildi; yüzde 11.6’ da yani 26 hastada da IMNM vardı, anti-HMGCR antikorları ise yüzde 6.9’ da pozitif idi.
IMM’ li 233 hastanın 36’ sı statin kullanıyordu; bunların 15’ i (%41.7) anti-HMGCR antikorlar vardı ve 13’ ünün (%36.1) kas biyopsilerinde nekrotizan miyopati belirlendi.
Anti-HMGCR antikorları olan 15 hastanın hepsi de statin kullanmıştı ama diğer 202 hastanın sadece 21’ inde statin kullanma hikâyesi vardı.
Tüm bu bulgular, statin kullanımı ile anti-HMGCR antikorları ve nekrotizan miyopati gelişimi arasında bir ilişki olduğunu gösteriyor.
Statinlerle ilişkili IMNM’ nın belirtileri, statin miyopatilerinde olduğu gibi ilaç kesildiğinde düzelmiyor, hatta çoğunda daha da kötüleşiyor ve ömür boyu devam ediyor.
Gelelim neticeye
Statin lobisi kolesterol haplarının dünyanın en emniyetli ilaçları olduğunu, ufak tefek (!) yan etkilerinin ilaç bırakılınca tamamen düzeleceğini söyler durur ama durumun gerçekte hiç de öyle olmadığı her geçen gün daha iyi anlaşılıyor.
Immun-mediated nekrotizan miyopatinin (IMNM) de statin yazan hekimlerin çoğu tarafından adının bile bilinmediğine eminim.
İlaç kesilse de belirtileri ömür boyu devam eden hatta çoğunda belirtilerin daha da kötüleştiği, immunsüpresif tedavi gerektiren bu tablonun sapasağlam insanların başına gelmesi tam anlamıyla bir felâket.
Leblebi yazar gibi statin yazan etıbbaya önemle duyurulur.
“Önce zarar verme” prensibini unutmayalım.
Kaynaklar
2. http://onlinelibrary.wiley.com/doi/10.1002/art.27572/abstract
3. http://www.ncbi.nlm.nih.gov/pubmed/?term=grable-esposito+p+katzberg+hd
4. http://onlinelibrary.wiley.com/doi/10.1002/art.30156/abstract
5. http://www.medpagetoday.com/Rheumatology/GeneralRheumatology/52416
Not: Bu yazı 5 numaralı kaynaktan özetlenmiştir.
***
EK 1 (15.9.2022): MARYANNE DEMASİ Do statins cause muscle aches?
Cholesterol-lowering medications called statins are widely prescribed, however, about 50% of patients dump their statins within a year of commencing therapy.
The most common complaint is muscle problems – pain, weakness, cramps, and aches.
But now, a major study published in The Lancet has concluded that statins are rarely to blame.
The study has garnered international media attention and left many patients wondering if their doctors will believe them if they complain about muscle pains after taking a statin.
The following analysis argues that the conclusion of this new study is misguided and highlights how the design of industry-funded statin trials has led to the obfuscation of muscle harms.
Who did the study?
The study was conducted by researchers from the University of Oxford’s Cholesterol Treatment Trialists’ (CTT) Collaboration.
The group famously entered into a legally binding agreement with the industry sponsors of the statin trials to allow it exclusive access to the ‘individual participant data.’
There was one condition though. The group could not share the trial data with third party researchers, thereby preventing independent scrutiny.
This has been a sore point for many independent researchers who say, science, by its very nature, requires contestability.
The CTT group sits under the umbrella of the Clinical Trial Service Unit (CTSU) at Oxford, an organisation that has received over £260million in research funding from the drug industry, the vast majority from manufacturers of cholesterol-lowering drugs.
The findings
The CTT’s meta-analysis of 23 randomised clinical trials involving 155,000 individuals, found that statins were not the cause of muscle pain in over 90% of those who experienced symptoms, and likely due to “other conditions” such as ageing.
In 19 trials of statin therapy versus placebo, there was less than a 1% difference in the number of people who reported symptoms (27.1% statins vs 26.6% placebo).
The rates of muscle harms remained consistent across different brands of statins and under different clinical circumstances, although higher doses were associated with a sightly higher risk.
The CTT group concluded that muscle symptoms are common in the population, and that any small increase observed with statins doesn’t outweigh the cardiovascular benefits.
Expert analysis
1. If you don’t look, you won’t find
A valid assessment of muscle harms will ultimately depend on whether the original trials were able to ascertain reliable rates of muscle pain in the placebo and statin arms of the trial.
Peter Doshi, Associate Professor at the University of Maryland School of Pharmacy said, “If the answer is ‘no’, then crunching the trial numbers together doesn’t really help us as we could be in a garbage-in, garbage-out situation.”
Doshi went on to say, “If a trial does not properly survey patients for a specific type of adverse event, the reported rates of those events may be completely unreliable. In other words, inadequate data collection can render the results ambiguous or meaningless.”
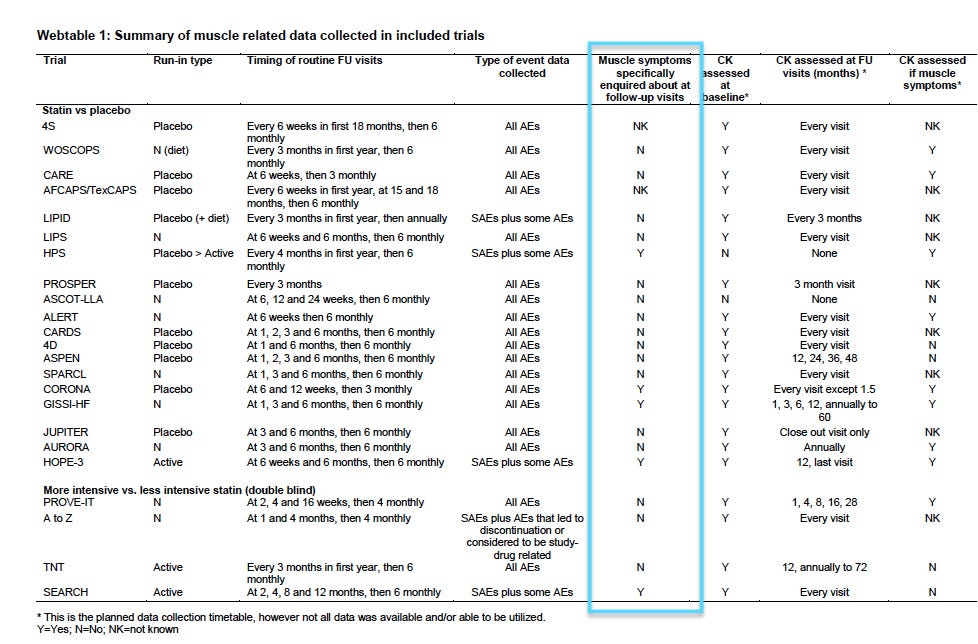
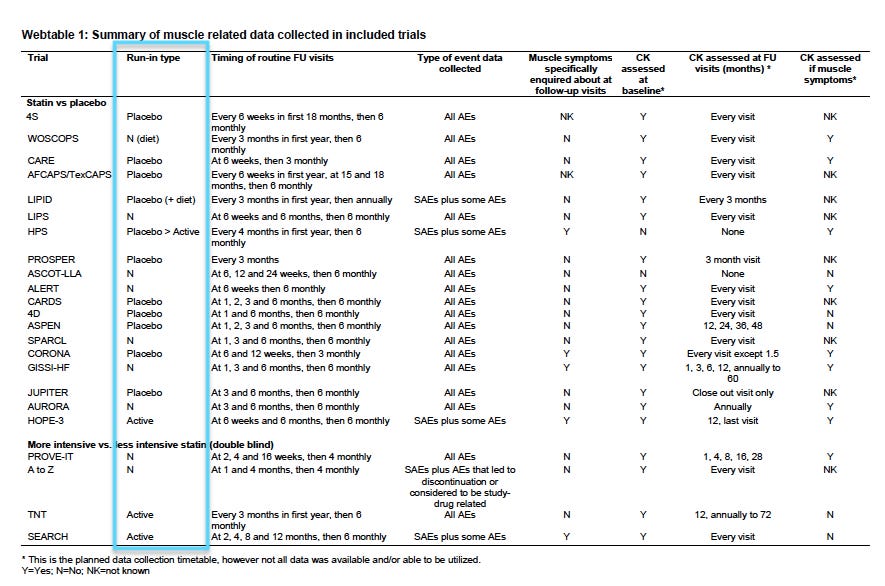
In the CTT analysis, the majority of statin trials – 78% (18/23) – either did not specifically enquire about muscle harms, or it remained unknown. (See Webtable 1).
Therefore, without active solicitation of muscle-related adverse events, a reliance on this type of passive surveillance system means that harms could occur without being documented.
Notably, there was no consistency in the way muscle harms were documented between statin trials and no defined criteria for labelling muscle harms, so aggregating the data in a meaningful way, was problematic.
The CTT authors acknowledged the limitation of their study:
The aggregate rate of reporting of any muscle pain or weakness (ie, for statin and placebo groups combined) during the first year of treatment varied substantially by trial (appendix p 10), from 1·0% to 60·5%, reflecting heterogeneity in how actively information was sought.
“That’s pretty extreme heterogeneity,” said Doshi.
The finding, however, was unsurprising to him. Doshi’s research team obtained statin trial data from Canada’s drug regulator to analyse the methods used to ascertain muscle-related events – their analysis of 23 trials was published recently in the J Gen Intern Med.
“Only 1 trial had such a dedicated surveillance and reporting system. Of the remaining 22 of 23 trials, we found they lacked adequate data collection methods to ascertain rates of muscle related adverse events,” said Doshi.
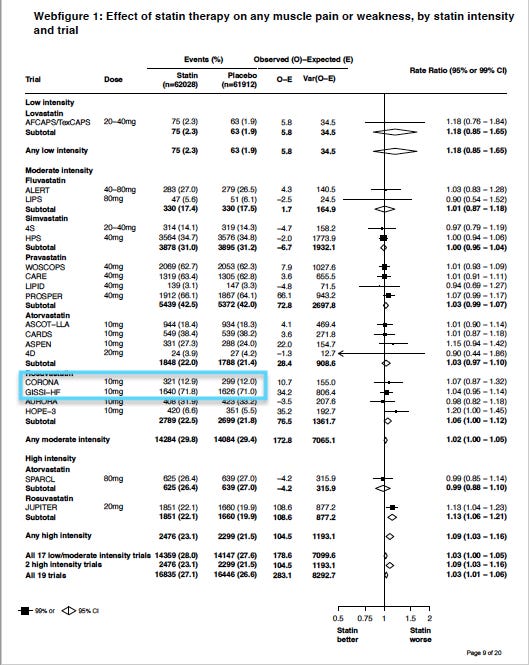
He pointed me to 2 major statin trials – CORONA and GISSI-HF. Both trials were designed similarly and recruited similar cohorts, i.e. patients with heart failure, but the placebo groups were strikingly different.
In the CORONA trial, the placebo group reported 12% muscle harms, compared to 71% in the GISSI-HF trial. (see Webfigure1)
Doshi said, “The wildly different rates in what seem like similar patient populations suggests that the determination of whether somebody has muscle symptoms is highly dependent on how the questions are asked by the trial investigator. That is rather problematic.”
2. Excluding trial participants
The exclusion criteria used in many statin trials has been the subject of intense criticism.
Beatrice Golomb, Professor at the University of California San Diego has questioned why the CTT analysis only included studies with a treatment duration of 2 years or more, excluding those with a shorter duration.
“What could have been the justification for this when they know that muscle pain is an outcome that usually emerges within the first couple of months after initiating a statin?” said Golomb, who has spent decades researching the impact of statins on muscles.
Golomb added, “What this ensures, is that only the largest trials, which are most likely to be industry-funded, are included in the analysis and smaller publicly-funded trials, are not.”
Golomb explained that it was possible to set criteria for selecting or excluding trials in a meta-analysis that would favour the benefits of the statin and underplay the harms.
She was highly critical of the CTT analysis because it included trials that used active “run-ins,” something she considered a design flaw in a trial, especially when analysing harms.
An active ‘run-in’ means that all potential subjects are given the active drug for several weeks and at the end of that period, anyone who was non-compliant or did not tolerate the drug, is excluded from the trial prior to randomisation.
“Effectively, you’ve selected out the people who will not comply with the drug, or who drop out because they experience muscle pain, so then muscle problems in the trial may be seriously under-reported,” said Golomb.
In the Heart Protection Study, for example, they removed 36% of participants from the trial once the run-in period was complete, and only those who remained were randomised to placebo or a statin.
“It’s brazen to do that and it’s so obviously distorting,” said Golomb.
Four trials in the CTT analysis used ‘active drug’ run-ins, while 10 trials used ‘placebo pills’ for the run-in period. (see Webtable 1)
Another way of obscuring muscle harms in statin trials, is to exclude participants who have a history of statin intolerance or those who have raised creatine kinase (CK) levels, an enzyme that indicates muscle damage when elevated.
In the CTT analysis of 23 trials:
-
2 trials excluded subjects with ‘statin intolerance’ (ASCOT-LLA, PROVE-IT),
-
4 trials excluded anyone with a known history of statin-induced myopathy (4D, CORONA, AURORA, JUPITER),
-
1 trial excluded people with known ‘contraindication to statins’ (HOPE-3), and
-
1 trial excluded anyone with a history of non-traumatic rhabdomyolysis (A-Z trial)
Further, 15 statin trials in the analysis excluded patients with elevated CK levels (mainly, CK levels >3x the upper limit of normal).
Obviously, the CTT analysis, which contained a significant proportion of trials that excluded participants who had experienced, or might’ve experienced, muscle problems would generate results that are not generalisable to the broader population.
Why is this important?
While muscle pain is not immediately life threatening to most people, it can adversely impact a person’s quality of life and limit mobility, particularly in the frail and elderly. Physical activity is a central preventive measure for heart disease, as well as many other diseases.
Typically, muscle problems reported in clinical trials have been described as ‘rare’ (<5%), but most clinicians I spoke with, even those who regularly prescribe statins, report the rate is closer to 20%.
Weighing up the benefits and harms of statins becomes critical when you consider that the majority of people prescribed statins are at low risk of heart disease (primary prevention).
“With trials, the devil is often in the detail — for example, I have no idea how data were collected from those who discontinued treatment because of side effects — and so ultimately I am left with questions, and I don’t feel we’ve gotten to the bottom of this issue of statin associated muscle symptoms,” said Doshi.
The implication of this new study is that patients who experience muscle harms after taking a statin are experiencing the ‘nocebo’ effect – i.e. the mere ‘suggestion’ that statins might induce muscle pain is making people imagine they have muscle pain, and negative media coverage is often blamed for that influence.
However, many patients who discontinue their statins notice that their symptoms resolve, and only return once they resume their medication.
“The experiences of patients who develop these symptoms on resuming a statin (rechallenge) must be kept in mind because a rechallenge is also a hallmark feature of causality determination,” said Doshi.
***
EK 2 (22.3.2023): Kolesterol hapının yol açtığı kas güçsüzlüğüne (miyopati) ilaç geliştirilmiş. Şimdi sıra kas güçsüzlüğüne iyi gelen ilacın müstakbel yan etkilerine karşı yeni bir ilaç geliştirmede. Hiç şüphem yok bunu da başaracaklardır.
Kaynak: https://www.jpost.com/health-and-wellness/article-735058
Makale: Israeli researchers develop medication to treat statin myopathy – study
Makale: Limb girdle muscular disease caused by HMGCR mutation and statin myopathy treatable with mevalonolactone,
***
EK 3 (18.10.2023): Are muscle aches from statins really due to the nocebo effect?
Kaynak: https://maryannedemasi.substack.com/p/are-muscle-aches-from-statins-really
***
EK 4 (7.3.2026): Yüksek doz (günde 80 mg) kolesterol hapı (atorvastatin), iskelet kasları mitokondri kapasitesinde çarpıcı ve ilerleyici bir düşüşe yol açıyor – 56 günde %30+ kayıp.
Bu kayıp kolesterol haplarının neden miyopati (kas zafiyeti) ve kas yorgunluğunun da sebebi olabilir.
▶Bu, statinlerin kas mitokondrisi üzerindeki ilerleyici etkisini insanlarda ilk kez net gösteren güçlü bir çalışma!
Mitokondriler sadece iskelet kaslarının değil tüm hücrelerin enerji santralidir.
Statinler, vücudun temel ayarlarının canına okuyor ! desek yeri var.
Kaynak: https://x.com/drahmetrasim/status/2030372043300950242?s=20
***
EK 5 (23.3.2026): Filim adamları uçana kaçana kolesterol hapı (statin) yutturmak için ellerinden geleni arkalarına koymazken bir tarafta da bu ilaçların en çok görülen yan etkisi olan kas zayıflığının (miyopati) nasıl giderilebileceğine kafa yoran bilim adamları var.
Uzun zamandır statin verilen her hastaya koenzim Q10 verilmesi de rutine girmişti ama bu takviyeler herkeste işe yaramıyor.
Bir hap içtim hayatım değişti diyen yazar haklı. Her içilen hap yeni haplara davetiyedir.
Aşağıda bu anlattıklarımın teknik izahatı var, meraklıları için:
Statinlerin koenzim Q10 sentezini de baskılayarak miyopatiye sebep olduğu kabul edilir ve hastalara bir de koenzimvQ10 takviyesi verilir. Gel gelelim, birden fazla meta-analiz bunun statin kaynaklı miyopati semptomlarını anlamlı derecede düzeltmediğini, belirgin bir fayda sağlamadığını gösteriyor.
Statinler, mevalonat yolunu bloke ederek geranylgeraniol (GG) ve GGPP -geranylgeranyl pyrophosphate) üretimini de azaltır.
Bu, küçük GTPaz proteinlerinin geranylgeranylation (prenilasyon) sürecini bozar; bu süreç kas hücresinin hayatta kalması, fonksiyonu ve atrofi önlenmesi için zorunludur (örneğin atrogin-1 gibi atrofi genlerinin aşırı aktivasyonu önlenir).
Koenzim Q10 yolun daha aşağı kısmında yer alır ve GG, koenzimQ10 sentezinin zorunlu substratıdır — yani GG takviyesi hem kök nedeni (prenilasyon eksikliği) giderir hem de CoQ10’u dolaylı olarak yeniler.
Kemirgen modelinde simvastatin kaynaklı iskelet kası yorgunluğunu GG (GGOH) takviyesinin tamamen önlediğini gösterildi. Bu etki hızlı kasılan (kaslarda belirgindi ve kalp kası veya damar düz kası fonksiyonunda advers etki yaratmadı.
Diğer hayvan modellerinde GG, statin kaynaklı atrofi ve kas hasarını tersine çevirdi (örneğin atrogin-1 ekspresyonunu baskılayarak).
Henüz büyük ölçekli, tamamlanmış klinik çalışma yok, ancak devam eden/annatto kaynaklı GG takviyesiyle statin miyopatisinde kas sonuçlarını inceleyen faz çalışmaları var.
In vitro, yani kas hücre kültürü ve hayvan çalışmaları tutarlı şekilde GG’ nin koruyucu olduğunu gösteriyor.
GG’nin miyopati yönetiminde umut verici olduğunu ve CoQ10’dan üstün olabileceğini vurguluyor.
Özetle, şu anki kanıtlar umut verici ama henüz standart tedavi tavsiyesi seviyesinde değil.
https://www.mayoclinicproceedings.org/article/S0025-6196(14)00799-X/fulltext
https://pubmed.ncbi.nlm.nih.gov/33999383/
https://www.sciencedirect.com/science/article/abs/pii/S1931524419301677
https://www.frontiersin.org/journals/physiology/articles/10.3389/fphys.2023.1246589/full
Kaynak: https://x.com/drahmetrasim/status/2036172493598187584?s=20
***















Hocam statinler hakkında yazmaktan onları kötülemekten bıkmadınız ama şu da bir gerçek ki bizlerin de gözlerini açtınız.
Artık statin yazarken eskisi kadar rahat değilim, aklıma hemen siz geliyorsunuz.
Hap içmediği için kalp krizi felç geçirenlerin veya ölenlerin sorumluluğunu alıyor musunuz yoksa ölen ölür kalan sağlar bizim mi diyorsunuz?
52 yaşındayım 30 senedir sigara içerim Askerde başladım Birinci sigarasıyla sonra Avrupa sigaralara alıştım. bana da kötü kolestorum yüksek diye hemen hap yazdılar fakat hocamı takip ettiğimden almadım. Doktorum almazsan enfaktüs geçirirsin pat diye ölürsün diye korkutmaya devam ediyor fakat ben gene de inatla almıyorum. O reçeteye yazıyor ben almıyorum evde bir koca kutu Lipitor hapı birikti. Sigarayı bıraktım her gün 1-2 saat de yürüyorum bu arada 4 kilo verdim 2 ay içinde ve kendimi de çok zinde hissediyorum taşı sıksam suyu çıkarırım alimallah. Allah senden razı olsun hıacam
Helal olsun hocam size, kolesterol haplarını rezili rüsva ettiniz. Doktorlar artık reçete yazarken eskisi kadar rahat değil. Babama da yazacaklardı ben doktor beye ama Ahmet Rasim Hoca bunun herkese gerekli olmadığını yan etkilerinin çok olduğunu söylüyor dediğim de adamcağız almasa da olur ama ben yazmak zorundayım dedi. yarın birgün babana bir şey olursa kalpten giderse mesela gelip benden hesap sorarsınız, ben ilacı yazarım baban ister içsin ister içmesin dedi. Aynen böyle oldu. Tıp bitmiş hocam sayende öğrendik Tıp tamamen satılmış. Bunda bence gariban doktorların da günahı yok. kapitalsit sistem böyle çalışıyor, yani kaba olacak ama yerse!
Kalp damarlarının tıkanması ile kolesterolün hiç bir ilişkisi gösterilmemiştir. Asrımızın en büyük, ticari yalanıdır!
Kolesterol ilacı yazmamaktan korkan hekimlerin içi rahat olsun, vebale falan girmezler, daha da faydalı olurlar hastalarına.
Kolesterol ilaçlarının kalp krizini önlediği henüz hiç bir bağımsız çalışma ile gösterilememiştir. Sizler ilaç firmalarının yaptırdığı ve yorumladığı sonuçlara göre ilaç yazmayınca nasıl korkuyorsunuz, telaşa kapılıyorsunuz? O denli beyniniz yıkanmış gibi geliyor bana.
Kalp krizi geçirenlerin yarısının kolesterol değerleri ya düşüktür yada normal (?) denilen düzeydedir.
Kan kolesterolü yüksek (?) olan insanların yarısı da yani %50 kadarı kalp krizi geçirmezler.
Kalp krizinin nedeni kan pıhtısıdır, PIHTIDIR; PIHTI. Anjio laboratuarında, kriz geçiren kişilerin damarını tıkayan kan pıhtısı eritilerek, damar açılır! Kolesterol pıhtı yapıyorsa neden kolesterol eritilmiyor acaba?
Ya da kol, bacak damarları ve internal meme arteri, sağlıklı ve sağlam diye, by-pass ameliyatlarında kullanıyor acaba? Aynı yüksek kolesterol (?) bu damarlara hiç uğramıyor mu? Neden tıkalı değiller!
Kalp krizinin nedeni KOLESTEROL falan değildir, bakın nelerdir.
Bir damarın tıkanması için binlerce faktörün bir araya gelmesi gerekmektedir. Bir okyanus gibidir insan vücudu da, okyanusun bozulmasında tek bir yosun diyelim, sorumlu olamaz, onu ortadan kaldırmanız ile okyanuzsun bozuk düzeni ve dengesi düzelmez, mümkün değildir.
Bağımsız bilim insanlarının, EUROPEAN WARF LONDON 2104 Bilimsel toplantı özeti:
1. Bütün kolesterol molekülleri faydalıdır ve hayati önemleri vardır.
2. Kolesterol sentezinin bloke edilmesi son derece zararlıdır.
3. Şekerlerin okside ettikleri LDL zararlıdır.
4. Az şekerli beslenme ile kan yağ profilleri normalleşmektedir.
5. Az yağlı bütün işlenmiş yiyecekler gizli şekerlerle doludur.
6. Füktoz, glükozdan 7X daha tehlikeli ve zararlıdır.
7. Kardiovasküler Hastalıklar, Obezite, Alzheimer ve Demans hastalıkları, ve Diabet komplikasyonları şekerlenerek bozulmuş proteinlerin-yani gliko-proteinlerin- belirtileridir.
Kaynaklar:
1. Wainwright G, Mascitelli L & Goldstein M R. Cholesterol Lowering Therapies & Membrane Cholesterol. Arch of Medical Science. Vol. 5 Issue 3 2009
2. Saher et al., Highest cholesterol content in brain is found in myelin. Nat Neurosci,8(4), 2005.
3. Thomas H. Haines. Do Sterols Reduce Proton and Sodium Leaks through Lipid Bilayers. Lower Cholesterol= Leaky Membranes Activation Failure & ‘Runaway Burn’. Progress in Lipid Research (2001) Vol.40, pp. 299-324.
4. Seneff S., Wainwright G., Mascitelli L. Is the metabolic syndrome caused by a high fructose, and relatively low fat, low cholesterol diet? DOI:1105114/aoms.2011.20598. Arch of
Önceleri Karayay’a da Küçükusta’ ya da çok kızıyordum hem halkın hem doktorların kafalarını karıştırıyorlar diye, bilhassa da Küçükusta’ ya. Bir göğüs hastalıkları uzmanı çıkmış her konuda ahkam kesiyor diye. Sen ne anlarsın kalpten kolesterolden diyordum ama yazılarını okudukça hepsinin bilimsel kaynak ve datalara dayandığını gördükçe hele de son kitabı Büyük kolesterol Yalanlarını okuyunca fikrim tamamen değişti. Bu iki değerleri hocanın binlerce meslekdaşına karşı kahramanca gerçek bilimi ve gerçek tıbbı savunduklarını gördüm. Onlara bir özür borcum var, teşekkürlerimle.
Dr. K.T. aramiza hosgeldiniz..:)
Keske adinizi tipki onlara kizarken de yaptiginiz gibi acikca yazsaydiniz
ilaçlar nasıl imal ediliyor.